媒体聚焦
新型冠状病毒肺炎重症超声应用专家共识(战时应急稿)(2020.03.02 搜狐新闻)
温馨提示
本文为本刊“COVID-19专题”系列文章,该系列文章内容均经过同行评议,将发表在《中国急救医学》杂志2020年3期,可作为有效引用数据。网络优先出版尚未完成完整编校流程,实际印刷版可能略有修改。本文引用格式:国家卫生健康委能力建设和继续教育中心,中国医学装备学会超声装备技术委员会战创伤和急重症超声专业委员会,中国医学装备学会超声装备技术委员会远程及移动超声专业委员会. 新型冠状病毒肺炎重症超声应用专家共识(战时应急稿)[J].中国急救医学,2020,40(3):0000.
新型冠状病毒肺炎重症超声应用专家共识(战时应急稿)
摘 要
针对新型冠状病毒(SARS-Cov-2)不同于既往流感病毒所致的肺炎传播,一场没有硝烟的防控疫情战役仍在进行。新型冠状病毒肺炎(Corona Virus Disease 2019,COVID-19),简称“新冠肺炎”。COVID-19具有传播迅速、进展快、危重症率高的特点。临床影像学检查主要依据胸部X 线、 CT 胸部扫描外,也可采用超声影像学检查。2020年2月初广东援鄂医疗队在无法使用听诊器的条件下,采用超声成功地诊断并抢救了一名生命垂危COVID-19老年患者。超声设备尤其是便携超声仪器,可以随时移动到病床旁进行检查,在 4G或5G 网络下,还可进行远程超声会诊,非常适合于隔离医疗区使用。由于超声探头与病人接触面小而更易消毒。从前线反馈的信息获悉,超声已在COVID-19的诊断、疗效评估、随访中发挥了不可或缺的重要作用。
【关键词】 COVID-19;超声;床旁评估;远程超声
1 什么是新型冠状病毒肺炎
起源于湖北武汉的新型冠状病毒(SARS-Cov-2)已导致全球八万人感染,其中重症率超过10%。SARS-Cov-2直径平均约120nm,而细菌则以微米为计量单位。病毒颗粒随呼吸进入气道和肺,会走得更远,直达细支气管和肺泡,导致本次COVID-19的病变多分布在胸膜下的终末端肺泡。COVID-19肺组织尸检病理表明病变肺泡呈弥漫性损伤,伴随细胞纤维粘液性渗出引起肺实变[1]。在CT上表现为双侧肺周边或近胸膜处的磨玻璃影,胸腔积液少见。COVID-19病变的分布特点易于被超声显示。
从临床角度看,发病早期外周血白细胞总数正常或减少,淋巴细胞计数减少,提示大量的淋巴细胞被消耗、患者抵抗力低,易合并细菌感染。一些患者表现为顽固性低氧血症,病毒感染还会引起全身其他器官的损伤,如心、肾损伤,临床上出现心率下降,复苏效果差。
2 超声可否用于新型冠状病毒肺炎的临床评估
2.1 肺超声检查的基本概念与成像基础
正常肺脏气体所占比例高达98%以上,因此在肺表面脏层胸膜处,气体与软组织间的巨大声阻抗差使得超声大部分被反射,仅能显示其表面。当肺脏病变引起肺脏正常气—液比例发生改变,并且累及到肺脏表面时,超声波能够在局部传播,形成特有的超声图像,以辅助诊断[2]。
2.1.1 声阻抗差:当界面大于波长,声阻抗差大于千分之一(1‰)时,即有回声反射,是超声成像的基础。反射波的强弱由两种介质的声阻抗差决定,即声阻抗差越大,反射越强(图1)。

注:A:界面大于波长时发生的回声反射示意图;B:胸膜线在二维超声图像中表现为强回声(箭头所示)
图1 声阻抗差
2.1.2 多重反射、混响效应:在两个平行的反射界面之间,声波可以多次往复反射并被探头接收,超声仪器可记录这些多次反射的回波,称为多重反射,或称混响效应。第一个反射回波为客观的位置,随后依次接收到回波的时间逐渐增加,距离相应增加。肺超声中的A线与此相关(图2)。
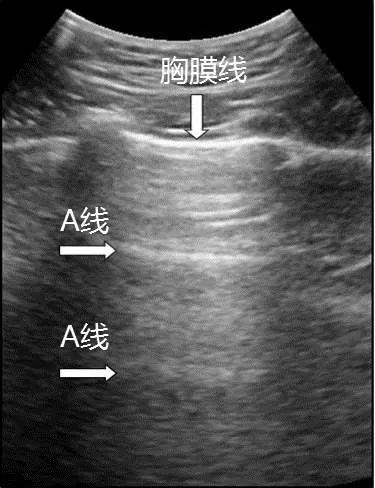
注:二维超声图中与胸膜线平行的为A线(箭头所示)
图2 A线
2.1.3 彗星尾征:在软组织中传播的声束遇到水气泡、小结晶等薄层强反射界面时,超声在其内部可产生多次反射直至衰减,反射的回声被探头接收,产生内部混响效应,即声像图显示的“彗星尾征”(图3)。
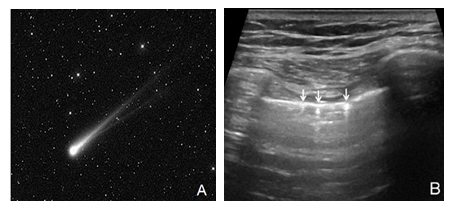
注:A:空中闪过的彗星尾图像;B:为二维超声图中肺表面的气体所产生的彗星尾征(箭头所示)
图3 彗星尾征
2.1.4 振铃伪像:超声波在气体包绕的液体之间产生强烈的震荡,产生连续的回波并被探头接收。其后方不衰减,似激光样,如肺超声中的B线(图4)。
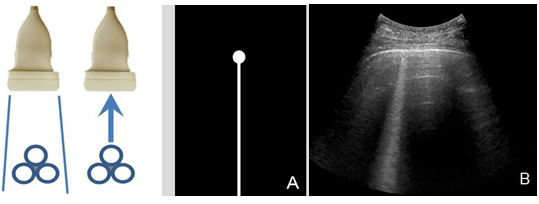
注:A:超声波在气体包绕的液体之间产生强烈的震荡,产生连续的回波并被探头接收;B:肺泡内气泡在超声激励下震荡并被探头接收,声像图中形成与胸膜线垂直的激光束样强回声,即B线(箭头所示)
图 4振铃伪像
2.1.5 M型超声:M型超声是采用单声束扫描的方法,使M型取样线依次穿过人体组织,取样线经过的组织回声随时间改变所形成的曲线以图像的形式显示出来。在肺超声及心循环容量评估中有重要价值(图5)。
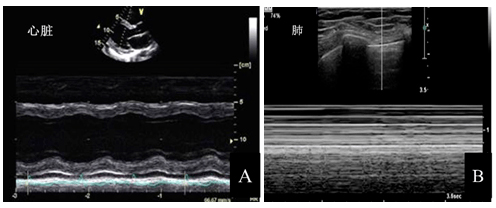
注:A:心脏的M型超声心动图;B:正常肺的M型超声图。纵轴(Y轴)代表距离;横轴(X轴)代表时间,将不同深度的组织回声随时间的运动展开,构成时间-运动曲线
图5 M型超声图像
专家意见:条款内容参照了肺超声成像原理的文献,结合了COVID-19 的临床实践经验,对重要的肺超声物理概念进行解释。
推荐强度:B. 推荐:循证证据肯定,能够提高肺超声应用的认识。
2.2 超声设备及其调节
2.2.1 超声设备:本次COVID-19由于传染性强,疫区疑似及确诊患者数量大,除了常规台式超声诊断仪,需要重视便携式超声的应用,甚至使用掌上超声、机器人超声,利用远程医疗平台连接一线疫区及后方医院。
2.2.2 探头及检查条件的选择:COVID-19主要针对心、肺进行检查,同时,由于重症患者可出现多脏器衰竭,因此,肝、肾等重要腹部实质脏器及血管超声也对患者的全面评估起着重要作用,尤其是下肢深静脉血栓的监测和困难患者的置管,超声的作用非常大。因此,COVID-19的超声检查,可能需要综合应用相控阵、凸阵、线阵等多种类型探头及心脏、腹部、血管、浅表器官等多种超声检查条件。
2.2.3 图像的存储与分析:为了减少超声医生的暴露时间,要求按照重症超声检查流程进行,快速、全面地采集动态及静态图像资料,离开感染环境后再行深入分析。
专家意见:条款内容参照了国内外文献,并结合临床实践经验,对仪器设备及成像参数条件等影响超声诊断的因素进行提示。
推荐强度:A. 强烈推荐:循证证据肯定,能够改善超声诊断和临床评估,减少漏诊及误诊。
2.3 新型冠状病毒肺炎的超声评估
2.3.1 正常肺超声征象及其病理征象
2.3.1.1正常肺脏声像图
①胸膜线:探头垂直肺脏表面扫查,声束在胸壁与脏层胸膜-肺表面交界处产生大量反射形成的强回声,称为“胸膜线”。
②A线:也称水平线。见图3。
③“蝙蝠”征:探头沿人体纵断面扫查,显示上下相邻两根肋骨及其肋间隙的肺脏,肋骨横断面强回声伴后方声影与肋间隙的胸膜线强回声一起形似展翅飞翔的蝙蝠,故称作“蝙蝠”征(图6)。灰阶声像图显示相邻两根肋骨及其声影、肺脏表面的胸膜线,三者类似展翅的蝙蝠。
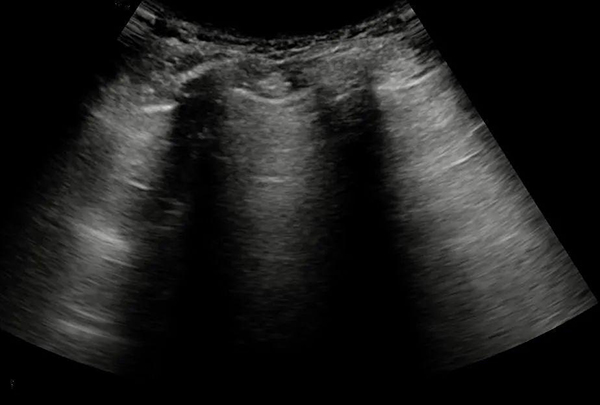
图6 肺脏超声的“蝙蝠”征
④肺滑动征:正常肺脏胸膜线强回声随呼吸运动节律,在实时超声上显示为相对胸壁的往返滑动,称为肺滑动征。
⑤“海岸沙滩”征:应用 M 型超声观察正常肺脏。由于肺脏实时运动,M型声像图上表现为弥漫的颗粒状中等回声,状如海岸边的沙滩。而相对静止不动的胸壁组织形成层状的线样强回声,宛如大海里面的层层波涛。故称之为“海岸沙滩”征(见图5B)。
2.3.1.2 常见异常肺脏声像图
① 肺滑动征消失当气胸时,游离气体不受肺脏呼吸活动控制,胸壁与气体之间的强回声界面呈相对静止状态,因重力原因浮于肺脏上方,掩盖了气体深方可能仍存在的正常肺滑动征。肺滑动征消失除气胸外,还见于胸膜黏连、重度肺纤维化、呼吸暂停、完全性肺不张等情况。
②平流层征或条码征肺滑动征消失的M型超声表现,此时肺脏滑动形成的颗粒状“沙滩”区域消失,代之以密集分布的平行线,酷似平流层或条码。
③肺点气胸时部分萎陷的肺脏仍然保持着吸气膨胀,呼吸回缩的动态变化。吸气时,肺脏膨胀,将胸腔游离气体推挤;呼气时,肺脏回缩,游离气体占据被推挤开的位置。二者相汇处的声像图呈动态交替变化,此位置即肺点。尽管肺点诊断气胸的敏感性较低(66%),但特异性高达(100%)。
④B线及其家族:肺泡、肺间质炎症渗出以及肺间质纤维化累及脏层胸膜,使肺脏表面出现液—气、组织—气声学界面,超声波激励后产生共振,出现振铃效应,在声像图上表现为点状强回声伴后方密集排列的窄带样强回声,远场不衰减,称作B线,也称垂直线,正常肺脏侧胸部临近膈肌的肋间隙可见B 线,数量不超过2~3 条。B3线与B7线:两条相邻B线的间距约3 mm时称作B3线,如果间距为6 ~7 mm则称为B7线。B7线间距与肺小叶解剖间隔距离基本一致,代表增多的液体渗出至小叶间隔。而每个肺泡直径约2 ~3 mm,B3线可能表明肺泡水平的液体聚集。B线密集排列难以区分计数,遍布整个肺野时,声像图显示为广泛的B线样强回声,称为白肺(图7)。

注:A:超声显示起源于胸膜线并与胸膜线垂直的彗星尾样强回声,此处B线间距约3mm,即B3线。B:B线密集分布,彼此分辨不清,甚至肋骨声影都受到干扰,整个肺野由“白色”高回声区域占据,称为白肺
图7 B线及白肺
⑤碎片征胸膜下局部肺泡内气体消失,肺泡腔内充满液体(渗出液、漏出液、血液等)形成实性变,实性变区域的肺组织与周围及深方含气肺组织的边界不清,交错分布,声像图呈现不规则的实性低回声区,状若碎片。
⑥实性组织征肺脏实性变区域累及整个肺段甚至肺叶,声像图类似实性软组织,边界清晰,内部可见肺脏血管形成的纹理,也称为肝样变。
⑦支气管气相和支气管液相肺实变时,局部支气管内残存气体或液体所产生的征象。如果支气管内残存气体随呼吸闪烁移动,则称为动态支气管气相。如果支气管内残存液体,则表现为沿管道分布的低至无回声。
⑧胸腔积液胸膜腔内积聚不同量的液体,超声显示胸腔内无回声区,后方回声增强,因病因不同,无回声区内可回声不均匀。大量积液时可见压缩的肺组织在积液内飘动。
专家意见:条款内容是结合超声物理原理,分析正常及病理状态下的肺超声成像特征,参考了国内外超声成像基础的文献。
推荐强度:B. 推荐:循证证据良好,能够有利于临床超声图像的分析和判断。
2.3.2 肺超声检查方法及步骤
对肺部的超声扫查,可以采用垂直胸壁平行肋间隙或垂直肋间隙做纵向和横向扫查,同一部位做连续性扫查。常用的超声检查方法和步骤可按照BLUE-PLUS方案、单侧6分区方案和8分区方案等。
2.3.2.1 BLUE-PLUS方案: 法国学者Lichtenstein总结出鉴于急诊床旁肺部超声的检查方案(Bedside lung ultrasound in Emergency, BLUE)。方法和步骤采用检查者的手型与胸壁的位置,形象设定BLUE和壁肺泡/胸膜综合征(PLAPS)点。 与CT比较,该方案可以发现大部分CT显示的肺外周型病变和胸膜病变[3-4]。其不足之处:超声检查点受检查者手型大小、患者的膈肌位置影响,存在一定误差。
2.3.2.1 单侧六分区方案和俯卧位单侧八分区方案: 将单侧肺以腋前线、腋后线为界,分为前肺、侧肺及后侧肺三个区,每个区再分为上下两部分,即前上、前下、侧上、侧下、后上、后下共六个区[5](图8)。针对COVID-19的肺部病变以双侧、周边、多灶,且肺泡内粘液较多的特点,可采用单侧八分区法进行肺部超声检查,多用于肺复张评估。在临床重症应用中,单侧六分区方案应用更广泛。
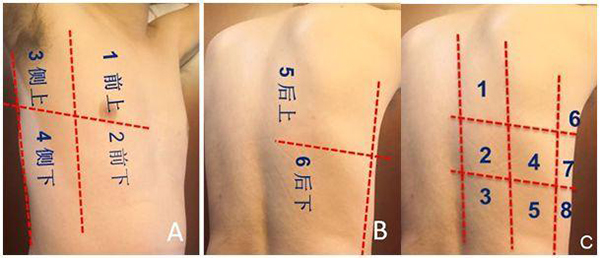
注:A和B:仰卧或侧卧位(右侧),以腋前线、腋后线为界,分为前肺、侧肺、后侧肺三区,每个区再分为上下两部分;C:俯卧位(右侧)以脊柱旁线、肩胛线和腋后线将背部分为3个部分,每个部分等分为上、中、下3个区,每侧除去被肩胛骨遮挡的区域,共16个检查区
图8 单侧六区方案的分区方法
专家意见:条款内容是参照国内外普通肺超声和重症肺超声的检查方法及步骤 ,分析了肺超声的检查几种分区法及步骤。
推荐强度:B. 推荐:循证证据良好,能够有利于临床超声图像采集,避免漏诊。
2.3.3 新型冠状病毒肺炎的超声特征
COVID-19 超声特征与其他病毒性肺炎、小叶性肺炎有类似之处,其超声表现随自然病程的发展而不同,是肺内气、水比例发生改变的超声体现,其特征主要表现为 (图9)。
2.3.3.1 胸膜线及A线:增厚、回声粗糙、中断,A线消失,肺滑动征减弱或消失。
2.3.3.2 B线:增多,B7线提示间质性肺水肿可能,B3线或更密集提示肺泡性肺水肿可能;B线融合形成白肺。
2.3.3.3 肺实变:胸膜下肺不张合并 B线征;肺实变伴碎片征、支气管充气征,当气体完全被吸收后,表现为肝样变。
2.3.3.4 胸腔积液:可有胸腔积液,但多为少量,或呈局限性。
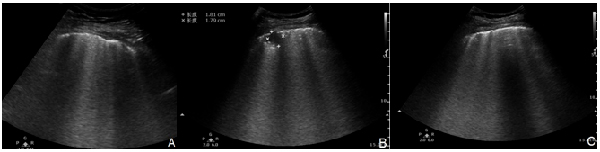
注:A:超声显示胸膜线增厚、欠光滑,A线消失,B线数量稍增多(箭头所示);B:胸膜下肺实变(测量游标所示);C:胸膜线增厚、回声中断,B线数量增多、融合,间隔≤3 mm
图9 COVID-19超声图像
2.3.4 COVID-19严重程度的超声评估
COVID-19肺部病变严重程度随病情发展时刻变化,并且多种超声征象可同时存在,交替变化,因此超声在床旁实时的评估病情进展变化及时调整治疗方案对患者有重要的临床价值。
2.3.4.1 COVID-19早期:一般感染患者发病后0~4天,偶有干咳,胸闷,低热等临床轻微症状[6]。肺周可见胸膜线欠光滑、模糊、中断;部分胸膜线下可见小斑片状低回声影,边界不清;胸膜线下可见多条B线或融合B线(呈瀑布征)[7],位置固定。单个或多个肺区局部累及。(图10)
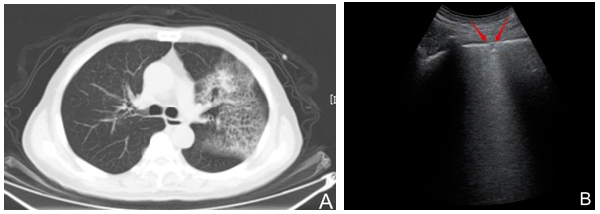
注:A:COVID-19患者,男,81岁,发热,体温最高37.8℃,HRCT显示左肺上野区肺周处胸膜下磨玻璃样团片影,内可见网状表现。B:超声凸阵探头显示左后下肺野区肺周宽大B线,A线消失,肺周小斑片样病灶,胸膜线不连续(红箭头所示)
图10 COVID-19早期影像表现
2.3.4.2 COVID-19进展期:一般患者发病后5~8天,伴有咳嗽,气短,发热等临床症状[6]。超声于肺周可见胸膜线中断;胸膜线下可见多发、连续斑片样、结节样、长条样低回声实变影,形态不规则;实变肺组织内可见细支气管充气征,病灶下可见多条B线或融合B线(呈瀑布征)[7],位置固定。单个或多个肺区累及,以双肺后下肺野为著。部分病灶相邻胸膜腔内可见局限性胸腔积液及增厚胸膜(图11)[8]。CDFI显示实变区域血流信号较常规肺炎病灶稀少。
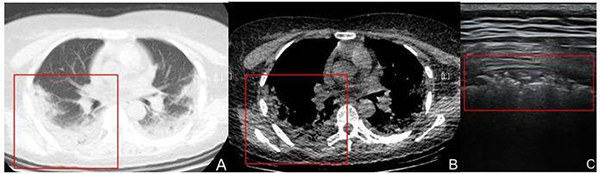
注:A和B:分别是肺窗、纵膈窗CT图像,COVID-19患者,女,42岁,发热7天,体温最高38.5℃,HRCT显示右肺后上野区肺周处胸膜下条带样实变影,内密度不均匀(红方框所示)。C:超声线阵探头显示右后上肺野胸膜线中断、消失,胸膜下可见条带样暗淡实变肺组织,其内可见散在细支气管充气征,后伴B线(红方框所示)
图11 COVID-19进展期影像表现
2.3.4.3 COVID-19重症期:患者发病后10~13天,伴有呼吸困难,发热等临床症状[6]。超声于肺周可见胸膜线中断或消失;胸膜线下实变范围进一步扩大,可见多发、连续大片样低回声实变影,部分呈“肝样变”[9];实变肺组织内可见支气管充气征或细支气管充气征,多个肺区累及,以双肺后下肺野实变为著,其他肺区亦可见较广分布大片条带样小斑片影,病灶后呈弥漫样B线分布,呈“白肺”征;部分病灶胸膜腔内可见游离胸腔积液及增厚胸膜(图12);CDFI超声显示实变区域内近肺门端实变病灶内可见树枝样血流信号,肺周实变区内血流信号不明显。
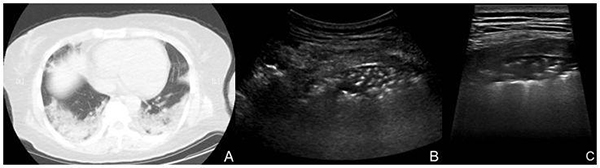
注:A:COVID-19患者,女,42岁,发热13天,体温最高38.5℃,CT显示病灶分布肺区广,双后侧肺野均可见大片状低回声实变影,内可见细支气管充气征。B和C:超声显示低回声的肺实变区,后伴融合B线
图12 COVID-19重症期影像表现
专家意见:条款内容介绍了COVID-19的超声特征及不同进展时期的超声表现,与胸部CT表现对照,均来自一线确诊病例。
推荐强度:A.强烈推荐:循证证据肯定,有利于提高COVID-19肺炎超声图像的认识、分析和判断。
2.3.5 COVID-19的心肌损伤及其超声特征
COVID-19重型患者病情进展迅速,约31%的危重型患者出现心脏损伤[10]。床旁超声心动图在COVID-19心-肺-血管联合诊断评估能及时协助临床医疗决策。
2.3.5.1 重型或危重型COVID-19患者的超声评估要点
①快速评估左心功能及右心功能:1)室壁运动正常患者推荐目测左心功能。2)室壁运动弥漫性减弱推荐M型方法评估左心功能。3)节段性室壁运动异常可采用单平面或双平面Simpson方法评估。4)必要时目测右室壁运动或M 型方法测量三尖瓣环收缩期最大位移TAPSE,二维方法估测右心室面积变化率RVFAC。
②评估肺动脉压力:在无右室流出道狭窄的情况下采用三尖瓣反流压估测肺动脉收缩压。
③评估下腔静脉的宽度和随呼吸的变化(见相关章节)。
④快速明确心包积液及定位:剑突下切面和胸骨旁切面。
⑤及时排查心脏结构异常、有无合并急性及慢性心脏疾病,不推荐全面的常规测量。
2.3.5.2 COVID-19心肌损伤的超声特征
①左心功能不全:左心增大,左室壁节段性或弥漫性运动减弱,收缩功能降低(图13);合并基础心血管疾病或诱发新出现的心血管疾病者出现相应表现,如心肌梗死并附壁血栓形成(图14A)。
②右心功能不全:右心增大,右心压力负荷升高,右心室收缩功能不全(图14B)。
③肺动脉高压:肺动脉主干增宽,右心增大;室间隔突向右室,三尖瓣反流压升高(图15)。
④心包积液及心脏压塞:心脏摆动,舒张期右室壁塌陷,吸气相室间隔向左室移动,下腔静脉扩张。
⑤提示心律失常,基础病和并发症的超声表现。
专家意见:条款内容是根据武汉协和医院超声科COVID-19患者床旁超声心动图像采集,分析了床旁超声心动图在COVID-19导致的心肌损伤中的诊断和评估的价值。
推荐强度:A. 推荐:循证证据肯定,能够改善临床结局,利大于弊 。
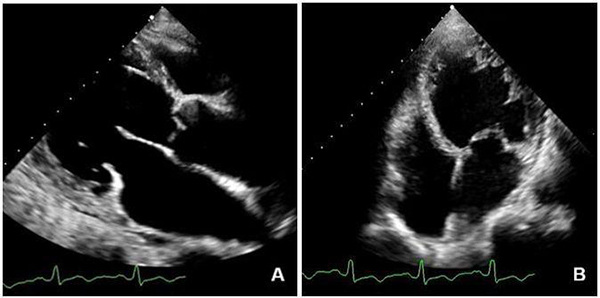
注:A:男性,73岁,病毒性肺炎,核酸检测阳性,CRP170 mg/L,BNP1077 pg/mL;A和B左心长轴和心尖四腔切面显示左心明显增大
图13 COVID-19 伴心脏异常
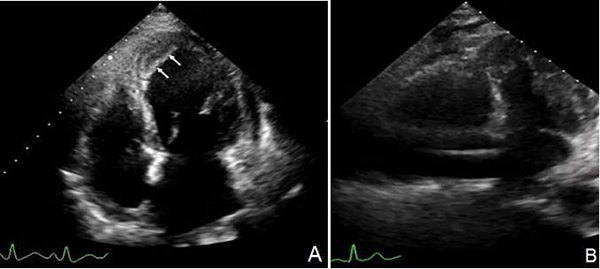
注:A:女性,45岁,病毒性肺炎,核酸检测阳性,D-二聚体 3.39 μg/mL,TnI 9889.4 ng/L,BNP632 pg/mL,心尖四腔心切面显示左室心尖室壁瘤伴血栓形成(箭头所示);B:男性,69岁,病毒性肺炎,呼吸衰竭,核酸检测阳性,D-二聚体 6.82 μg/mL,BNP632 pg/mL,心尖四腔心切面显示右心明显增大
图14 COVID-19伴心脏异常
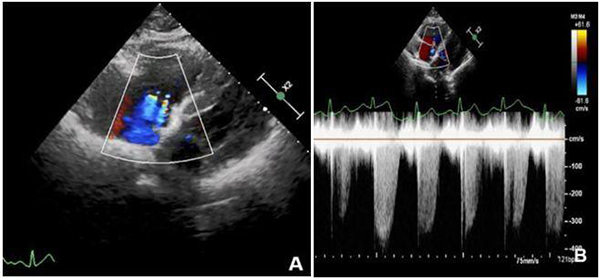
注:与图14B为同一患者,A:彩色多普勒显示三尖瓣反流;B:三尖瓣反流频谱估测肺动脉收缩压增高。
图15 COVID-19 合并肺高压
2.3.6 小儿肺
目前,认为小儿也是COVID-19的易感人群,且肺超声在儿科的应用相对成熟。超声还可鉴别其他常见儿科肺脏疾病,如新生儿呼吸窘迫综合征(NRDS)、胎粪吸入综合征、新生儿暂时性呼吸增快症和新生儿气胸等。
正常肺脏超声影像特点:与成人肺部超声相同,详见前述。需注意的是,新生婴儿可在出生3-7天内部分肺野出现稀疏B线,随着发育,于几天后消失(图16)。
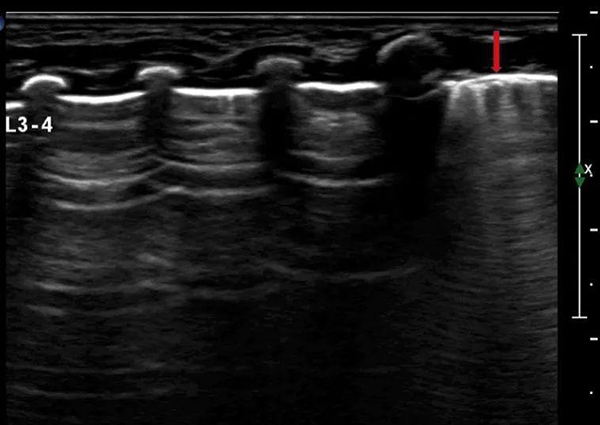
注:超声可在局部肺野出现稀疏B线(箭头示)
图16 新生儿肺超声检查
新生儿肺部疾病的超声主要表现:①肺野出现胸膜线增厚、模糊、连续性中断征,A线消失。②肺野内出现密度程度不等的B线,从稀疏B线到融合B线,肺泡-间质综合征,甚至“白肺”。③肺实变,伴或不伴有支气管气相、支气管液相。可局限于胸膜下,呈形态不规则、大小不等的低回声区,内夹杂斑片样、雪花样气体强回声,或“碎片征”等,较大的实变可呈团块状。④不同程度的胸腔积液,单侧或双侧均可发生。⑤恢复期,可见原有实变区缩小,B线密度逐渐减低、消失,不同区域出现“双肺点”征,即A线、B线交界处,提示正常和水肿区域的分界点(图17)。
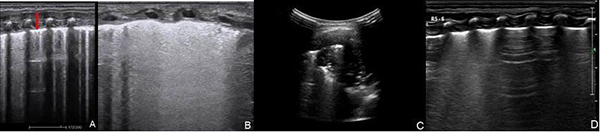
注:A:超声显示肺野胸膜线增厚、模糊(箭头示),A线消失;B:不同密度的B线代表不同程度的肺泡-间质综合征改变,甚至“白肺”样变;C:肺实变,至肺野深部,呈块状;D:超声显示肺点,即正常肺组织和含水量增多的组织分界处
图17 新生儿肺超声检查
专家意见:条款内容介绍了小儿肺炎的超声表现及鉴别诊断。
推荐强度:B.推荐:循证证据肯定,能够有利于临床超声图像的分析和判断。
2.3.7 重症超声血容量评估
容量评估包括容量状态及容量反应性的评估。容量状态是指患者的前负荷状态,即心室的舒张末期容积,为静态指标。超声常见评价指标有左室舒张末期内径(LVEDD)及容积(LVEDV)、下腔静脉内径等。低血容量患者下腔静脉内径变窄,自主平静呼吸状态下,下腔静脉直径<9 mm,提示低血容量。LVEDD<35 mm,或出现乳头肌亲吻征等,同样提示可能容量不足。
容量反应性即心脏的前负荷反应性,是指扩容后的效果,是前负荷和心功能状况的综合反映,为动态指标。扩容后心输出量(CO)或每搏输出量(SV)较前增加≥10~15%,提示容量反应性好。超声常见评价指标有下腔静脉直径随呼吸变异度、左室流出道速度时间积分呼吸变异度(ΔVTI)及SV变异度(SVV)等[11-12]。下腔静脉变异度常通过塌陷指数(cIVC)及扩张指数(dIVC)体现[13]。cIVC=(Dmax-Dmin)/ Dmax,自主平静呼吸状态下,cIVC>40%,提示患者对补液治疗可能有效。无自主呼吸的机械通气状态下,下腔静脉的呼吸变异度公式dIVC=(Dmax-Dmin)/Dmin,临界值为18%。根据心肺交互作用或利用呼气暂停试验、被动抬腿试验或液体负荷试验,监测SVV、左室流出道ΔVTI同样是评估容量反应性的重要指标,临界值为12%~15%。
ΔVTI 计算公式为:
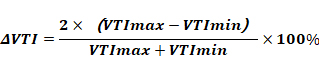
需注意的是,超声指标可应用于容量或容量反应性评估,但不能完全替代其他评估手段,如血压、中心静脉压、肺动脉楔压、持续心输出量监测(PiCCO)等,需互相结合进行综合分析。
2.3.8 介入超声
2.3.8.1 浆膜腔积液
COVID-19引起浆膜腔积液(包括胸腔、腹腔及心包腔积液)的病例较少,但重症患者出现多脏器衰竭,也可有多浆膜腔积液。超声可明确诊断,并根据临床需要行介入性超声治疗。
①适应证:游离性或包裹性浆膜腔积液者;需抽取积液进行化验以明确诊断者;需要引流和注药治疗者。
②禁忌证:有严重凝血功能障碍者;积液量极少者(<1.0 cm);无穿刺路径者。
③体位:胸腔积液患者多取坐位,包裹性胸腔积液者可采取任意体位;腹腔积液及心包积液者可取半卧位、平卧位或侧卧位。
④操作步骤:常规消毒、铺无菌巾,1%~2%利多卡因局麻。超声探头涂抹耦合剂后置于一次性无菌套内,超声引导下PTC针经皮穿刺至积液内,实时监视针尖位置,用注射器回抽液体,针尖逐步后撤,直至积液完全消失。需置管引流者,穿刺成功后,可用Seldinger法置管(图18、19),具体步骤为:回抽见到积液—拔出针芯—插入导丝—拔出针鞘—扩张针道—沿导丝置入引流管—退出导丝—连接引流袋[14]。
⑤常见并发症:超声实时引导,并发症少见,偶有感染、出血、周围脏器损伤。
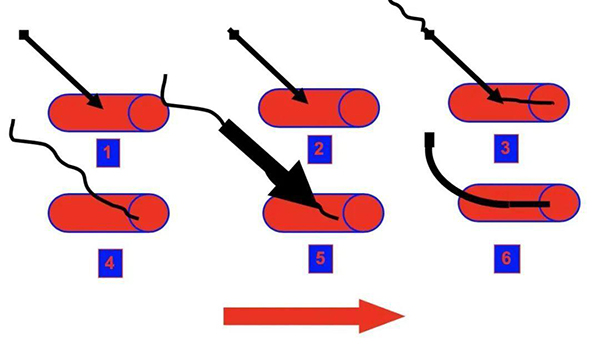
图18 Seldinger法穿刺置管示意图
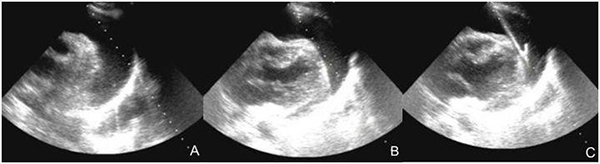
注:A:确定积液位置;B:置入穿刺针;C:置入引流管
图19 超声引导下心包积液穿刺置管
2.3.8.2 外周及中心静脉超声引导下穿刺、置管
在急危重症抢救中,超声引导外周及中心静脉置管可快速建立静脉通道[15-16]。
①适应证:静脉盲穿困难,急需采集血液标本或静脉内输液;需长期中心静脉置管;需溶栓等。
②禁忌证 :多发血栓性静脉炎、静脉通路不通畅或损伤者;其他同“浆膜腔积液穿刺禁忌证”。
③操作步骤:采用Seldinger法置入。步骤同“浆膜腔积液穿刺置管”。避免在原穿刺点反复穿刺,以免误伤动脉以及发生血肿、出血。穿刺置管后,必须关闭调节夹,防止空气进入形成气栓[17]。
④并发症:超声实时引导,并发症少见,偶有皮下气肿、心律失常、血栓形成。
2.3.8.3 超声在ECMO中的应用
体外膜肺氧合(extracorporeal membrane oxygenation, ECMO),也就是体外膜肺。ECMO的核心部分是膜肺和血泵,分别起人工肺和人工心的作用。经过气体交换的血液,在泵的推动下回到静脉(V-V模式),或回到动脉(V-A模式)[18]。当采用V-A模式时,多要经股动脉和股静脉插管;当采用V-V模式时,多要经股静脉和颈内静脉插管[19]。
超声引导动脉、静脉穿刺置管步骤:采用Seldinger法(图20)。V-A模式时,为避免向心股动脉内置管引起同侧肢体远端缺血,常需要建立远端动脉灌注管,此时因为股动脉内已有一导管,股动脉远端管径变细,血流减少,超声引导穿刺更准确、有效。动脉、静脉插管后,即刻超声实时观察导管尖端到达恰当位置,以发挥最佳临床效果。如经下腔静脉,下腔静脉应到达近右心房口处。
使用ECMO过程中,超声随时评价心功能和肺水;撤机前超声判断肺复张,肺心评价指标详见相关章节[20]。
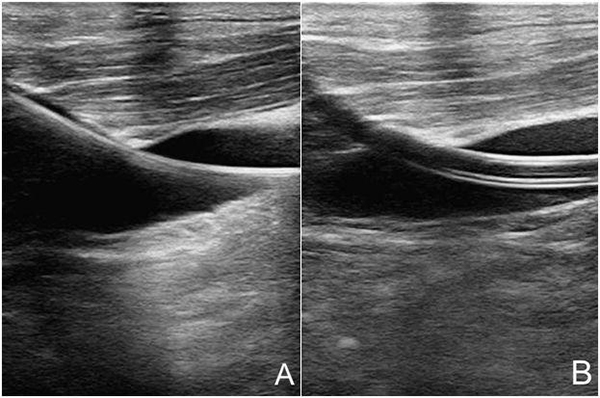
注:A:超声引导下沿着穿刺针置入导丝(箭头所示);B:超声引导下沿着导丝置入导管(箭头所示)
图20 超声引导颈内静脉穿刺置管术
专家意见:条款内容是参照国内外关于介入超声的 应用方法及步骤 ,结合了大量的临床工作实践。
推荐强度:A. 推荐:循证证据肯定,能够改善临床结局,利大于弊 。
2.4 超声医生防护
在超声诊疗过程中,医师与患者近距离密切接触,暴露程度有时甚于临床医师。超声医生防护分为如下区域进行。
2.4.1 超声普通诊区
2.4.1.1 诊区划分为:清洁区、缓冲区、污染区、员工通道、缓冲通道。医护人员上班经员工通道进入清洁区放置随身物品后,进入缓冲区穿工作服及防护用品后进入诊室;检查完成后,人员由诊室经缓冲通道进入缓冲区脱工作衣,进行手卫生后进入清洁区。
2.4.1.2 分诊、候诊区
①分诊人员自身防护:二级防护,保持环境通风,及时手卫生。
②分诊管理:患者进候诊区前需测体温并询问病史,发热及疑似患者均不能进入普通诊区。
③候诊管理:提醒患者及陪护分散就坐并配戴口罩;住院、门诊患者安排不同区域候诊。
2.4.1.3 诊室
①医护人员在普通诊室检查时穿戴工作服、工作帽、医用外科口罩,必要时加穿隔离衣及护目镜,戴乳胶手套或执行手卫生。
②诊室物品表面及地面可用含氯消毒液擦拭,每天2次;每日通风2~3次,每次不少于30分钟,可用空气消毒机或紫外线照射消毒。
③诊室使用一次性检查床单,每位患者检查前需更换;检查结束后探头清洁、消毒,做到一人一清洁、消毒。诊室内垃圾均装入医疗垃圾专用袋,按照《医疗废物管理办法》处理。
④已排除COVID-19的发热患者需安排单独诊室检查。
2.4.2 隔离病房
①进入隔离病房,遵守隔离区医护人员防护要求,按三级防护标准主要包括,一次性工作帽、护目镜(防雾型)或防护面屏、医用防护口罩(N95)、一次性防护服、隔离衣、一次性乳胶手套, 一次性靴套及鞋套,有分泌物或污染物喷溅时,加用全面型呼吸器防护器。②穿、脱防护流程(图21)。③脱卸的防护装备放入指定的一次性物品收集袋集中处置,参照《医疗废物管理条例》和《医疗卫生机构医疗废物管理办法》。
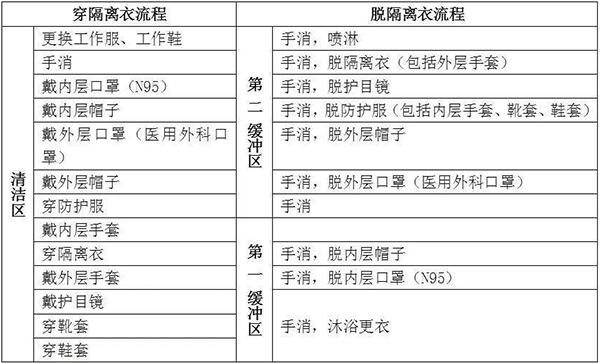
图21 穿、脱防护的流程图
2.5 超声设备的隔离与消毒
消毒时需佩戴手套和护目镜,避免消毒剂接触皮肤和眼睛。
2.5.1 主机的控制面板和显示器
消毒前先关机,使用含有消毒液湿巾或将消毒液喷洒在消毒部位用柔性清洁布擦净。注意勿过多喷洒消毒液,防止消毒液渗入控制面板操作接缝处。
2.5.2 探头
超声检查时建议使用一次性探头套,结束后取下一次性探头套,纸巾擦净探头,避免交叉感染。探头表面使用含有季铵盐类或过氧化氢的消毒剂擦拭消毒。
消毒液推荐:①主机及电缆线消毒:70% 异丙醇(IPA)或者75%的酒精;②探头消毒:戊二醛(2.0~2.5%)或者邻苯二甲醛(0.55%)。
专家意见:超声医师重点防护遵守隔离区医护人员防护要求;疫情期超声医学科需做好诊区管理和人员防护。
推荐级别:A级.强烈推荐:超声医护人员从自身防护的细节做起,防患于未然。
3 远程超声是否能在COVID-19疫情防控中发挥作用
远程超声是指利用信息化、互联网、AI、云计算、5G等技术,将超声设备上的图像传输至远距离的服务器或云端,在远距离通过调阅数据实现数据管理、远程会诊、后台分析、反向操控等功能。可以实现超声数据的异地实时共享与超声影像数据的互传互联[21]。
3.1 基本架构
远程超声的基本架构、数据管理模式图(图22)。通过远程超声的云平台,可以实现超声图像DICOM数据即刻存储/调阅、上传/下载、分析/归档。
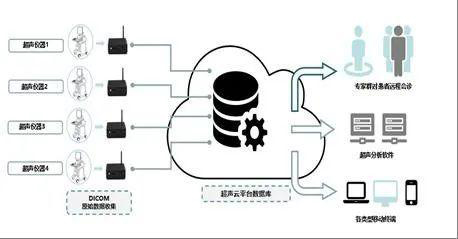
图22 远程超声的基本架构示意图
3.2 远程超声在COVID-19中的应用
超声检查时超声医师紧贴患者,容易感染。针对此次疫情,远程超声可以减少医师接触患者的机会。远程超声与机器人超声联合使用,能最大限度避免超声医生因为深入隔离病房导致的交叉感染,更便于重复动态观察病情。如肺心功能、容量评估,引导各种介入操作等(图23、24)。
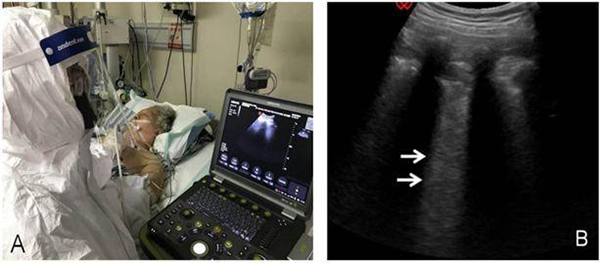
注:A:患者,女性, 67 岁,确诊COVID-19,患者端的医生进行肺超声检查,由会诊端医生给出会诊意见;B:左前胸上 BLUE 点显示 B 线显著增多、融合(箭头所示),局部胸膜增厚、欠光滑
图23 COVID-19患者的远程超声会诊
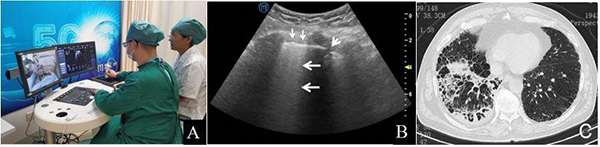
注:A:患者,男性,75岁,疑似COVID-19,远程超声检查,医生端的医生操作远程的患者端机器臂,两地直线距离1755km;B:右胸后外侧壁超声图像显示B线显著增多,出现B3(大箭头所示),局部胸膜增厚、欠光滑(小箭头所示),胸膜下显示小片肺不张区(箭簇所示);C:胸部CT显示右肺近胸膜处不规则条索、斑片状密度增高影及实变影,边缘模糊,以右肺下叶分布为主,病灶内见充气支气管影
图24 疑似COVID-19患者的5G远程机器人超声检查
远程超声的不足:①远程机器人超声的会诊医生需要操作手法的熟练度;②普通远程超声对患者端扫查医生的手法依赖性大,对图像标准化要求相对高。在数据安全和伦理方面,数据传输是远程超声系统应用的前提,医疗大数据具有特殊性,医疗数据的丢失、损毁、泄露、不当使用既是伦理问题,也是法律问题。
专家意见:条款内容参考了国内外专家的实际经验和文献报道。
推荐强度:B. 推荐:循证证据良好,能够有利于保证远程超声的可持续性规范化发展。
4 结论
从COVID-19疫情前线反馈的信息获悉,除了X线、CT等影像外,超声技术在此次战役中发挥了不可或缺的作用。其原因在于:超声设备便携,人能到的地方仪器就能到,手提超声可以方便地放置在隔离病房,掌上超声也可以置于口袋,随身携带;在4G或5G网络支持下,远程超声可以进行如身临其境般的远程会诊,适合隔离的医疗区使用。由于SARS-Cov-2存在空气和接触传染,而超声设备的隔离和消毒较CT、DR机有较大的优势,部分替代了听诊器。超声技术已在COVID-19的诊断、治疗及疗效评估中发挥较大价值。
证据等级与推荐强度:本专家共识各项条款内容均有相应的文献支撑依据,或根据编写组专家们成熟的临床实践经验。依据惯例对不同等级的证据赋予相应的推荐强度(见表1),以充分突出循证医学的科学理念。
表1 证据等级与推荐强度证据等级推荐强度A强烈推荐:循证证据肯定,能够改善临床结局,利大于弊B推荐:循证证据良好,能够改善临床结局,利大于弊C推荐:基于专家意见D反对推荐:基于专家意见E反对推荐:循证据良好,不能改普临床结局或弊大于利F强烈反对推荐:循证证据肯定,不能改善临床结局或弊大于利I不推荐或者不作为常规推荐:推荐或反对的循证证据不足、缺乏或结果矛盾,利弊无法评估
附件:急重症COVID-19超声检查报告单

编写组:
国家卫生健康委能力建设和继续教育中心
中国医学装备学会超声装备技术委员会战创伤和急重症超声专业委员会
中国医学装备学会超声装备技术委员会远程及移动超声专业委员会
审阅专家:杨爱平, 毓星, 王金锐, 孟庆义
编写人员(按姓氏笔画):
王金锐北京大学第三医院
叶瑞忠浙江省人民医院
吕发勤中国人民解放军总医院海南医院
刘禧空军军医大学空军特色医学中心
刘杰中国人民解放军总医院海南医院
杨爱平国家卫生健康委能力建设和继续教育中心
吴盛正中国人民解放军总医院海南医院
杨希武汉科技大学附属汉阳医院
孟庆义 中国人民解放军总医院第一医学中心
钱林学首都医科大学附属国际银河线路检查中心
徐辉雄上海同济大学附属第十人民医院
涂滨广州中医药大学附属佛山市中医院
贾化平解放军战略支援部队特色医学中心
崔立刚北京大学第三医院
寇海燕中国人民解放军总医院第三医学中心
黄毅西安市胸科医院
谢明星华中科技大学同济医学院附属协和医院
彭成忠浙江省人民医院
毓星国家卫生健康委药具管理中心
秘书:单雪霞,赵诗月 中国人民解放军总医院海南医院
参考文献(上下滑动)
[2] Rouby JJ, Arbelot C, Gao Y, et al. Training for Lung Ultrasound Score Measurement in Critically Ill Patients [J]. Am J Respir Crit Care Med,2018,198(3): 498-401.
[3] Lichtenstein DA, Meziere GA. Relevance of lung ultrasound in the diagnosis of acute respiratory failure: the BLUE protocol. Chest. 2008, 134: 117-125.
[4] Lichtenstein DA. Lung ultrasound in the critically ill [J]. Ann Intensive Care, 2014, 4(1): 1.
[5] Lichtenstein DA. BLUE-protocol and FALLS-protocol: two applications of lung ultrasound in the critically ill [J]. Chest, 2015, 147(6): 1659-1670.
[7] Dietrich CF, Mathis G, Blaivas M, et al. Lung B-line artefacts and their use[J]. J Thorac Dis, 2016, 8(6): 1356-1365.
[8] Wang G, Ji X, Xu Y, et al. Lung ultrasound: a promising tool to monitor ventilator-associated pneumonia in critically ill patients [J]. Crit Care, 2016, 20(1): 320.
[9] Inglis AJ, Nalos M, Sue KH, et al. Bedside lung ultrasound, mobile radiography and physical examination: a comparative analysis of diagnostic tools in the critically ill [J]. Crit Care Resusc, 2016, 18(2): 124.
[10] Huang C, Wang Y, Li X, et al. Clinical features of patients infected with 2019 novel coronavirus in Wuhan, China. lancet. 2020,395(10223):497-506.
[11] Miller A, Mandeville J.Predicting and measuring fluid responsivenesswith echocardiography[J]. Echo Res Pract,2016,3(2): G1-G12.
[12] Wu C Y, Cheng Y J, Liu Y J, et al.Predicting stroke volume andarterialpressure fluid responsiveness in liver cirrhosis patients using dynamicpreload variables: A prospective study of diagnostic accuracy[J]. EurJAnaesthesiol,2016,33(9): 645-652.
[13] 张青,刘大为,王小亭,等.超声观测不同部位下腔静脉内径及其变异度的研究[J]. 中华内科杂志,2014,53(11):880-8
[14] Liang SJ, Tu CY, Chen HJ, et al. Application of ultrasound-guided pigtail catheter for drainage of pleural effusions in the ICU. Intensive Care Med. 2009;35(2):350-354.
[15] Piton G, Capellier G, Winiszewski H. Ultrasound-guided vessel puncture: calling for Pythagoras' help. Crit Care. 2018;22(1):292.
[16] Saugel B, Scheeren TWL, Teboul JL. Ultrasound-guided central venous catheter placement: a structured review and recommendations for clinical practice. Crit Care. 2017;21(1):225.
[17] Shrestha GS. Longing for better ultrasound-guided subclavian/axillary venous cannulation. Crit Care. 2018;22(1):148.
[18] Bhoumesh Patel, Subhasis Chatterjee, SeannaDavignon, et al. Extracorporeal membrane oxygenation as rescue therapy for severe hypoxemic respiratory failure. J Thorac Dis. 2019; 11(Suppl 14): S1688–S1697.
[19] Carles Bautista-Rodriguez, Joan Sanchez-de-Toledo, Eduardo M. Da Cruz. The Role of Echocardiography in Neonates and Pediatric Patients on Extracorporeal Membrane Oxygenation. Front Pediatr. 2018; 6: 297.
[20] Hanneke IJsselstijn, MaaykeHunfeld, Raisa M. Schiller, et al. Improving Long-Term Outcomes After Extracorporeal Membrane Oxygenation: From Observational Follow-Up Programs Toward Risk Stratification. Front Pediatr. 2018; 6: 177.


